-
黑龙江高考多少分能上武汉大学(2024年) 武汉大学2024年在黑龙江的录取分数线
2025-06-30
-
黑龙江高考多少分能上厦门大学(2024年) 厦门大学2024年在黑龙江的录取分数线
2025-06-30
-
黑龙江高考多少分能上同济大学(2024年) 同济大学2024年在黑龙江的录取分数线
2025-06-30
-
黑龙江高考多少分能上南京大学(2024年) 南京大学2024年在黑龙江的录取分数线
2025-06-30
-
黑龙江高考多少分能上中国人民大学(2024年) 中国人民大学2024年在黑龙江的录取分数线
2025-06-30
怎么区分氧化反应和还原反应,如何去判断"氧化还原反应"?(化学)
大学排名更新时间:2024-02-04 15:25:36作者:高三网关注度:
氧化反应和还原反应的区别
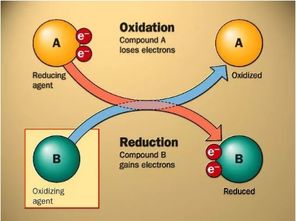
1、对氧的需求量不同。
氧化反应在于有机物反应时把有机物引入氧亦或是脱去氢的作用,还原反应却是起到将物质引入氢或失去氧的作用。
2、氧化值的变化不同。
氧化反应氧化时氧化值升高,而还原反应还原时氧化值降低,两者属于一高一低。
3、性质不同。
氧化反应失电子的性质是还原性,还原剂具有还原性。
还原反应得电子的性质是氧化性,氧化剂具有氧化性。
注:氧化剂和还原剂的确定是以实际反应为依据的,是相对而言的。
同一物质处于中间价态的在不同条件,不同反应中,可以作还原剂,也可做氧化剂。
如何去判断"氧化还原反应"?(化学)
氧化还原反应是在反应前后,某种元素的氧化数有变化的化学反应。
这种反应可以理解成由两个半反应构成,即氧化反应和还原反应。
复分解反应都不是氧化还原反应
置换反应都是氧化还原反应
有单质参加的化合反应一定是氧化还原反应
有单质生成的分解反应一定是氧化还原反应
另外要注意,有单质参加反应的化学反应不一定是氧化还原反应,如氧气生成臭氧
概念
反应的本质是氧化数有变化,即电子有转移。
氧化数升高,即失电子的半反应是氧化反应;氧化数降低,得电子的反应是还原反应。
氧化数升高的物质还原对方,自身被氧化,因此叫还原剂,其产物叫氧化产物;氧化数降低的物质氧化对方,自身被还原,因此叫氧化剂,其产物叫还原产物。
即:
还原剂 + 氧化剂 ---> 氧化产物 + 还原产物
一般来说,同一反应中还原产物的还原性比还原剂弱,氧化产物的氧化性比氧化剂弱,这就是所谓“强还原剂制弱还原剂,强氧化剂制弱氧化剂”。
凡例
氢气与氯气的化合反应
氢气与氯气的化合反应,其总反应式如下:
H2 + Cl2 → 2HCl
我们可以把它写成两个半反应的形式:
氧化反应:
H2 → 2H+ + 2e-
还原反应:
Cl2 + 2e- → 2Cl-
单质总为0价。
第1个半反应中,氢元素从0价被氧化到+1价;同时,在第2个半反应中,氯元素从0价被还原到?1价. (本段中,“价”指氧化数)
两个半反应加合,电子数削掉:
H2 → 2H+ + 2e-
+ 2e- + Cl2 → 2Cl-
---------------------
H2 + Cl2 → 2H+ + 2Cl-
最后,离子结合,形成氯化氢:
2H+ + 2Cl- → 2HCl
与电化学的关系
每一个氧化还原反应都可以做成一个原电池。
其中发生氧化反应的一极为阳极,即外电路的负极;还原反应的一极为阴极,即外电路的正极。
两个电极之间有电势差(电化学上通常叫电动势),因此反应可以进行,同时可以用来做功。
名称来源
氧化反应最早是指金属或非金属与氧结合形成氧化物的反应,这类反应中另一种元素的氧化数总是升高。
还原反应最早是指金属从其化合物中被提炼出来的反应,这类反应中金属的氧化数总是降低。
再如工业炼铁的反应:
Fe2O3+3CO=高温=2Fe+3CO2
这个反应中,三氧化二铁是氧化剂,而一氧化碳是大家熟悉的还原剂.三氧化二铁中的氧元素给了一氧化碳,使后者氧元素含量增加变为二氧化碳.铁由3价变为单质0价(降低,为氧化剂),而碳由2价变为4价(升高,为还原剂)
另外,复分解反应一定不是氧化还原反应.因为复分解反应中各元素的化合价都没有变化.例如:
Na2CO3+CaCl2=2NaCl+CaCO3(沉淀)
其中钠元素保持1价,碳酸根保持-2价,氯元素保持-1价,而钙元素保持2价.
氧化和还原反应的区别
1、性质不同:氧化-还原反应是化学反应前后,元素的氧化数有变化的一类反应。
氧化反应是物质与氧发生的化学反应,氧气在此过程中提供氧。
2、特征不同:物质与氧缓慢反应缓缓发热而不发光的氧化叫缓慢氧化,如金属锈蚀、生物呼吸等。
氧化还原反应前后,元素的氧化数发生变化。
根据氧化数的升高或降低,可以将氧化还原反应拆分成两个半反应。
3、氧化反应不同:镁在氧气中燃烧:2Mg + O2=2MgO 白色信号弹,发出耀眼的白光,放出热量,生成白色粉末。
大多数无机复分解反应都不是氧化还原反应,因为这些复分解反应中的离子互相交换,不存在电子的转移,各元素的氧化数没有变化。
标签:
相关文章
为您推荐
最新文章
- 黑龙江高考多少分能上武汉大学(2024年) 武汉大学2024年在黑龙江的录取分数线
- 黑龙江高考多少分能上厦门大学(2024年) 厦门大学2024年在黑龙江的录取分数线
- 黑龙江高考多少分能上同济大学(2024年) 同济大学2024年在黑龙江的录取分数线
- 黑龙江高考多少分能上南京大学(2024年) 南京大学2024年在黑龙江的录取分数线
- 黑龙江高考多少分能上中国人民大学(2024年) 中国人民大学2024年在黑龙江的录取分数线
- 黑龙江高考多少分能上中山大学(2024年) 中山大学2024年在黑龙江的录取分数线
- 2024年内蒙古高考227分左右的理科大学 2023年内蒙古高考227分的理科大学
- 208分左右的公办本科大学概览 青海职业技术大学
- 黑龙江高考多少分能上对外经济贸易大学(2024年) 对外经济贸易大学2024年在黑龙江的录取分数线
- 2024年内蒙古高考225分左右的理科大学 2023年内蒙古高考225分的理科大学
- 208分左右的民办本科大学概览 浙江广厦建设职业技术大学
- 黑龙江高考多少分能上北京航空航天大学(2024年) 北京航空航天大学2024年在黑龙江的录取分数线
- 2024年内蒙古高考224分左右的理科大学 2023年内蒙古高考224分的理科大学
- 208分左右的公办专科大学概览 克孜勒苏职业技术学院
- 黑龙江高考多少分能上北京大学(2024年) 北京大学2024年在黑龙江的录取分数线
- 黑龙江高考多少分能上上海交通大学(2024年) 上海交通大学2024年在黑龙江的录取分数线
- 黑龙江高考多少分能上清华大学(2024年) 清华大学2024年在黑龙江的录取分数线
- 黑龙江高考多少分能上上海财经大学(2024年) 上海财经大学2024年在黑龙江的录取分数线